抗体验证的优越策略:封闭肽验证
据报道,每年因劣质抗体造成的生物和医学研究损失约为8亿美元。此外,实验结果不一致和抗体重复性差的后果 是无法估计的。
国际抗体验证工作组(IWGAV)于2016年9月发表题为《 自然方法 中 抗体验证的建议》的文章 ,强调抗体验证应根据目标蛋白的相应应用和背景进行。作者提出了抗体验证的五个概念支柱:(i)遗传策略,(ii)正交策略,(iii)独立抗体策略,(iv)标记蛋白的表达,以及(v)免疫捕获后进行质谱分析。多发性硬化症)。
这五种方法各有其优缺点以及适用条件。例如,遗传策略通过比较细胞或组织中的相关信号来评估抗体特异性,其中使用 CRISPR-Cas9 或 RNA 干扰 (RNAi) 敲除或敲低目标基因与野生型 (WT) 对照的信号。尽管这种方法很简单,但未能击倒或敲除目标基因将大大损害该方法的实验可行性。
免疫捕获后进行质谱 (MS) 的方法可以识别与纯化抗体直接相互作用的蛋白质, 以及与目标蛋白质间接相互作用的其他蛋白质。 然而,这种方法依赖于昂贵的科学仪器和实验材料。并非每个实验室都能负担得起这些设备。
在 Affinity Biotech,抗体通过 独立抗体验证进行验证。为此,使用几种抗体来识别靶蛋白上的不同表位。具有最高特异性的抗体是通过包括比较和定量分析的适当程序确定的。虽然大多数抗体的检测应该没有问题,但对于检测特异性要求较高的抗体,特别是那些位点特异性的磷酸化抗体,仍然不够。
结合多年的抗体研发和生产经验,Affinity Biotech采用了更合适的抗体验证策略: 封闭 肽验证。
封闭肽(抗原)与抗体一一对应。 。这是最原始的材料,只有原厂才能提供。
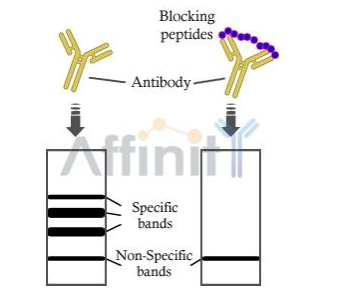
首先,我们对封闭肽进行 MS 分析,以确保肽序列准确。
在蛋白质印迹分析中,肽会阻断目标抗体的信号。没有封闭肽的泳道用作对照。封闭肽将与靶蛋白竞争结合位点,从而在封闭基团中不留下特异性条带。
该策略目前用于验证我们的抗体。它对于磷抗体的生产至关重要,因为它确保了磷抗体的位点特异性。换句话说,磷酸化抗体只能识别相应位点的磷酸化靶蛋白。非磷酸化的目标蛋白或其他位点磷酸化的目标蛋白将不会被识别。
举个例子。在 Phospho-MSK1 (Ser211) Antibody(货号 AF7155)的蛋白质印迹验证中,泳道 1 和泳道 3 中分别添加了非磷酸化阻断肽和磷酸化阻断肽。 2号车道没有被封闭。结果显示,使用磷酸化肽封闭目标蛋白后,没有检测到目的条带。