五元含氮杂环硼酸及其酯的合成
在过去的几十年中,偶联反应已广泛用于合成新型烷基化合物或芳香杂环化合物。
在这些过渡金属催化的偶联反应中,铃木偶联反应因其反应条件温和、适用于多个官能团、在空气中相对稳定和相对较低的毒性而受到青睐[1]。因此,化学家们一直对新型硼酸衍生物的合成和活性感兴趣。这些化合物,特别是含氮杂环硼酸,可用于药物化学研究中组合化合物库的建立。
五元含氮杂环硼酸及其酯的合成
1. 1 吡咯硼酸盐及其酯类的合成
早在1991年,吡咯硼酸盐衍生物的合成研究就开始了。但目前国内外发表的报道仍然很少。吡咯硼酸可以通过吡咯直接锂化或金属卤素置换和再硼化来制备,但这通常需要在氮原子上有一个保护基团。迄今为止,吡咯环上氮原子的保护基团主要是:叔丁氧羰基保护基[2]、三异丙基硅基保护基[3]、苯磺酰基保护基[4]。
1.1.1 2-吡咯硼酸及其酯的合成
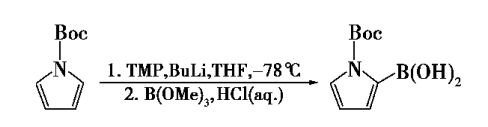
1991年,Schluter等人[2]报道了N-叔丁氧羰基-2-吡咯硼酸的合成,该酸是在-78°C下以N-叔丁氧羰基吡咯为起始原料制备的。 将2,2,6,6-四甲基哌啶在四氢呋喃中的溶液与正丁基锂反应,再与硼酸三甲酯反应生成相应的硼酸盐化合物,然后在酸性条件下水解即得目标。该产品的产率约为40%,如下所示。
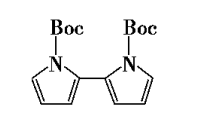
1993年,Kelly等人[5]以同样的方式制备了N-叔丁氧羰基-2-吡咯硼酸,收率为82%。近年来,其他研究小组以N-叔丁氧羰基吡咯为底物,在-78°C的四氢呋喃溶液中与LDA或LiTMP反应,通过硼酰化反应和水解反应得到N-un。丁氧羰基-2-吡咯硼酸的收率分别为58%、72%。已经发现硼酸化合物在铃木偶联反应中的应用的一个主要问题是加热容易脱硼,此外还形成一定量的二聚体,如下图所示。
为了减少铃木偶联反应中N-叔丁氧羰基-2-吡咯硼酸的脱硼反应和二聚化反应,Ketcha等[6]使用苯磺酰基作为氮原子的保护基团。然而,在1-苯基磺酰基吡咯2碳原子的锂基发生时,脱磺酰化反应竞争性地发生,最终得到相应的吡咯硼酸,收率仅为8%。2004年,Dinsmore等[7]在二异丙胺存在下制备了与底物相同的化合物,然后与异丙基溴化镁进行格氏反应,然后进行硼化和水解。对应的目标化合物,但收率仅为13%。
2002年,宫浦研究小组[8]报道了基于吡咯的2-吡咯硼酸频哪醇酯的合成,在铑催化剂二氯氯-1,5-环辛二烯基钌络合物和配体4,4'-二叔丁基-2,2'-二吡啶存在下,用二硼酸频哪醇以67%的收率生产相应的目标产物, 如下所示。在该反应中,用硼酸的频哪醇酯代替频哪醇二硼酸盐生成2-吡咯硼酸频哪醇酯,但收率降低到42%。研究发现,这种反应的主要问题是需要消耗大量过量的底物以避免二硼化产物的形成。
1.1.2 3-吡咯硼酸及其酯的合成
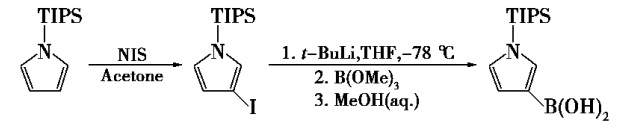
1992年,Muchowski等人[3]合成了1-三异丙基硅基-3-吡咯硼酸。该方法从三异丙基硅基吡咯开始,首先在吡咯的3位选择性碘处使用NIS,然后在叔丁基锂的作用下使用三甲基硼酸盐进行。反应在甲醇水溶液中进一步水解,得到所需的产物,其可以通过重结晶进一步纯化,如下所示。
2001年,Smith等[9]报道了在钌催化剂的作用下,在环己烷溶剂中将三异丙基硅基吡咯与硼酸频哪醇酯反应直接合成N-三异丙基硅基-3。- 吡咯硼酸盐法,收率81%。所述合成反应钌催化剂采用CpRh(η4-C6Me6)(其中Cp为五甲基环戊烯)。N-三异丙基硅基-3-吡咯硼酸频哪醇酯也可在反应中用频哪醇二硼酸盐代替硼酸酯,但收率为79%。
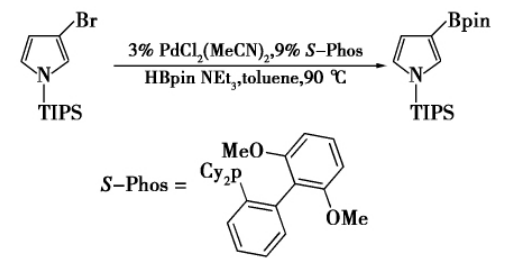
近年来,Buchwald研究小组[10]报道了金属钯的催化偶联制备1-三异丙基硅基-3-吡咯硼酸频哪醇酯,其为3-溴-N-三异丙基硅基。吡咯是一种底物,由硼酸频哪醇酯在S-Phos和三乙胺存在下作用产生,如下所示。此后,通过用叔丁氧羰基或苄基取代氮原子上的保护基进行相同的反应,但结果不尽如人意,收率仅为30%和24%。