嵌合抗体简介
嵌合抗体构建体被许多研究人员视为中间分子,但已逐渐被人源化抗体和人类抗体等更有效的分子取代。如今,这些结构嵌合体仅占批准用于临床的所有抗体的 10%。尽管如此,这些构建体的生产仍然充当抗体人源化过程中的中间体,并且偶尔充当研究和诊断中免疫测定的对照和校准物。
什么是嵌合抗体以及它们是如何产生的
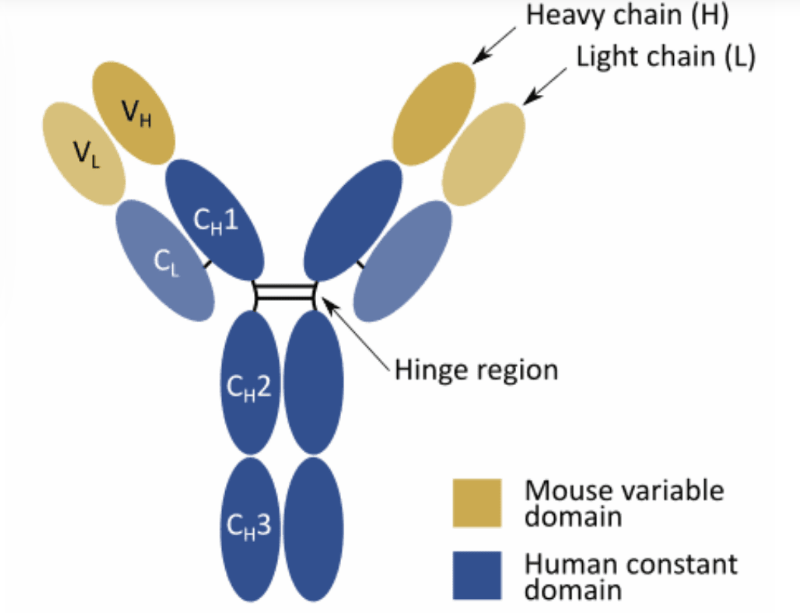
通过将来自一种宿主物种(例如小鼠、兔、美洲驼等)的抗体的可变结构域与来自不同物种(例如人)的抗体的恒定结构域融合,可以容易地产生嵌合抗体。这些结构嵌合体最初是为了最大限度地减少人抗小鼠抗体(HAMA)反应而开发的,当异种分子给予人类患者时,这种反应会损害抗体治疗的效率。
随着重组技术的出现,这些结构嵌合体的生产变得非常简单。通常,它们可以通过首先获得表达针对特定靶标的异种抗体的多个杂交瘤细胞系来产生。随后从这些细胞系中分离出 mRNA,并对可变域进行扩增和测序。
一旦我们确定了可变结构域的序列,我们就可以将它们与来自不同物种的抗体的恒定结构域组合,并在合适的表达系统(例如哺乳动物、微生物、植物或昆虫细胞系)中重组表达嵌合体。
嵌合抗体的应用
1997年,抗CD20嵌合抗体利妥昔单抗(MabThera)成为第一个被FDA批准用于治疗癌症的药物。利妥昔单抗成为成功的抗癌生物治疗药物之一,并经常用于治疗多种疾病,包括不同的血癌和自身免疫性疾病。
但截至 2020 年 3 月,只有 8 种其他嵌合抗体获得 FDA 或 EMA 批准,仅占目前临床使用的所有抗体的 10% 多一点。
最新获得批准的嵌合抗体是 isatuximab (Sarclisa®),旨在靶向 CD38(ADP-核糖基环化酶 1)。由ImmunoGen和赛诺菲-安万特公司开发的嵌合小鼠/人IgG1分子目前正用于治疗复发难治性多发性骨髓瘤患者。此外,这种抗体可能被证明可有效治疗血液恶性肿瘤。
与人源化抗体和人类抗体相比,嵌合抗体的批准率下降,反映出开发嵌合抗体用于临床应用的兴趣下降。然而,在许多情况下,嵌合分子仍然广泛应用于抗体人源化策略的初始阶段。由于人源化抗体仍占获得临床批准的大多数抗体(47%),因此嵌合中间体的生产仍然非常重要。
除了临床之外,嵌合抗体已被证明是免疫测定开发(例如 ELISA)的有用工具。由于这些嵌合构建体可以使用重组技术轻松生产,因此它们通常优于免疫测定中基于血清的校准品或对照品。它们也被证明可用于临床诊断。
例如,旨在检测患者样本中特定抗体的血清学免疫测定通常依赖于血清阳性血浆作为校准物或对照。然而,血清也有与多克隆抗体相同的缺点:
-
批次间差异
-
扩大生产或获得高滴度困难
-
表征方面的局限性
使用重组产生的嵌合抗体可以实现这些重要对照和校准品的可扩展性和标准化。此外,研究表明它们与人血清具有相当的反应性。因此,这些嵌合体代表了一种重要的妥协,使研究人员能够获得用于其测定的活性和标准化抗体,而无需将它们人性化,这将加剧这些试剂的成本和开发时间框架。
